适配体在手性药物拆分中的应用(一)
发布时间:2022-08-18
一、什么是手性
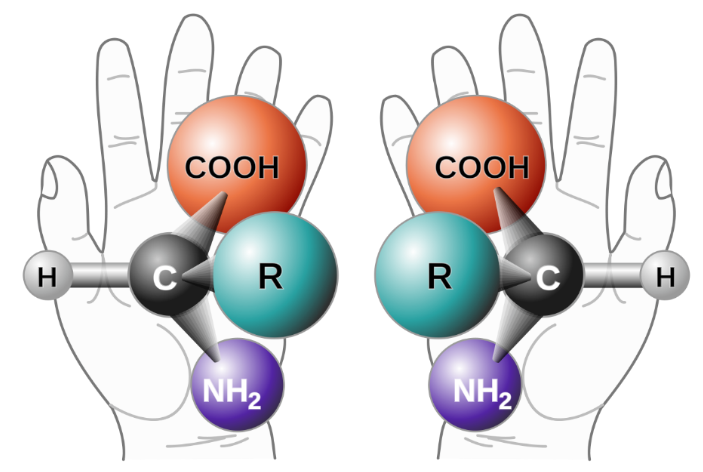
手性是非重叠能力的性质,含有不对称取代碳的分子称为手性分子(手性通常用左手和右手的概念来说明:左手和右手是彼此的镜像,但不可重叠)。
手性化合物在非手性环境中拥有相似的物理化学性质,但是在生物手性环境中,其中一种表现出符合预期的生理活性,而另外一种对映体则会表现出较弱的生物活性,负面效应甚至是毒性。比如:(S)-布洛芬被发现作为环氧合酶1的抑制剂比(R)-布洛芬强100倍以上。
二、手性药物拆分的意义
对于手性药物不够全面的了解导致了著名的“反应停事件”——沙利度胺是手性分子,右旋异构体具有镇静作用,能在妇女妊娠期控制精神紧张,防止孕妇恶心,并且有安眠作用;左旋异构体具有抗血管生成的作用,会影响妊娠初期胎儿某些器官的血管生成从而造成畸形。
但抗血管生成的作用使得沙利度胺左旋异构体可在抗肿瘤等方面发挥巨大作用,2006 年 5 月美国食品药品管理局( FDA) 批准其用于治疗多发性骨髓瘤,同时它也可用于肾癌、胶质细胞瘤、转移性黑素瘤的治疗。
因此有效地拆分手性药物不仅有助于提高生理活性和药理作用,而且有利于减少副作用。这对于手性药物和其他手性生物活性物质的实际应用具有极其重要的意义。
三、手性药物的传统拆分方法
1、色谱法拆分手性药物
色谱法作为传统使用的的分离方法,在手性药物的分离中得到广泛的应用,其中高效液相色谱(HPLC)、毛细管电色谱(CE)、气相色谱(GC)和超临界流体色谱(SFC)被认为是分离和测定手性化合物最有效、最方便的方法。
以高效液相色谱为基础,分离手性药物对映体可分为直接法与间接法。直接法分为手性流动相添加剂法(CMPA)和手性固定相法(CSP),间接法又称为手性试剂衍生化法(CDR),其中CSP法是最有效实用的方法。
CPS是由具有光学活性的单体固定在硅胶或其它聚合物上制成的,在拆分中CSP直接与对映体相互作用,与其中一个生成具有不稳定的短暂的对映体复合物,造成两种对映体在色谱柱内保留时间的不同,从而达到分离的目的。
环糊精(CDs)是一类重要的手性选择剂,是由α-1,4-糖苷键连接的吡喃葡萄糖单体组成的环状寡糖,可用于多种分子的对映体拆分。修饰的β-CDs可以借助衍生的基团来提高其手性识别能力,li课题组借助乙二胺衍生基团提供的静电相互作用和氢键作用,提高了β-CD的手性识别能力,实现了对5种丹酰化氨基酸对映体的高效分离。并且利用逆流色谱法,实现止吐药物ondansetron的对映体分离。CDs也可以通过纳米颗粒的修饰来提高对映体的分离选择性,CD修饰的金纳米粒子( CD - GNP)通过共价键合到硫代聚合物上形成的多孔整体柱可用于CEC中对映体的分离。该柱对于佐匹克隆、氯苯那敏和托吡卡胺三对药物对映体有着良好的分离效果。
Protein-based CSPs是另一类固定相,目前常用的固定相包括alpha-1-acid glycoprotein、bovine serum albumin和cellobiohydrolases CSs。Mallik 等人通过巯基将蛋白质及其他配体固定化在二氧化硅填料上制成固定相,其中HAS作为被键合的模型蛋白在HPLC 中显示出高亲和力,实现了对手性药物华法林和布洛芬良好分离。纳米材料在手性识别中具有独特的优势,因此Xu等人利用氨基修饰的介孔氧化硅纳米粒子(NH2-MSN),制备了一种poly(GMA-EDMA-NH2-MSN) 基质柱,之后以pepsin为CS,对15种基本手性药物的对映体进行分离,其中9种药物实现基线分离,6种药物部分分离。
分子印迹聚合物(MIPS)是以目标分子作为模板而制备的高分子聚合物,对目标分子具有高度的特异性识别能力,因此,非常适合于手性药物的拆分和纯化。Yue等人制备了MIPS涂层,该涂层具有良好的亲水性,能在水溶液中获到很好的分散,其作为分离介质对外消旋Trp有较好的分离度。Chen等通过AIBN热引发反应制备了MIPs开管柱,该开管柱实现了对普萘洛尔外消旋体的手性拆分。
除了以上几种手性识别剂固定相,许多生物材料可以在某一种特定的微环境中对目标分子有强烈的特异选择性。Li的团队就首次将南极假丝酵母脂肪酶B(CALB)作为一种新型CSP应用于CEC手性分离。Fu等利用细菌粘附特性和强静电相互作用,实现氧氟沙星对映体的基线分离和洛美沙星对映体的部分分离。Sun等利用溶菌酶的相变作用,制备了溶菌酶组装超分子膜修饰的开管电色谱柱,分离了肾上腺素、异丙肾上腺素和特布他林对映体。
2、酶拆分法
酶拆分法是利用酶对底物中某一对映体的立体选择性催化,使得一种对映体能够更快地生成产物,实现手性拆分。
在手性药物的拆分中,由于大部分药物的低水溶性,酶的非水相反应效率十分关键,在现有的研究当中,已知多种水解酶类,酯酶、脂肪酶、酰胺酶、腈水合酶、酰化酶等均能用于外消旋体的拆分,其中脂肪酶(lipase)应用较多、效果较好。
脂肪酶是一种重要的手性拆分酶,它在催化不对称合成时对底物有立体选择性,利用酶活性位点与两个底物对映体的立体选择性不同以及由此引起的两底物对映体反应速度的差异将两者进行拆分。Li等利用脂肪酶AK高效拆分了外消旋α-丙二烯并实现了克级拆分。
固定化酶的应用克服了酶易失活、难回收的不足, 能够保持甚至提高酶的活性, 延长酶使用寿命, 并且易于回收, 可重复使用。Liu等探究不同固定化方式对皱褶假丝酵母脂肪酶( Candida rugosa lipase,CRL) 活性的影响,结果表明聚集涂层固定的酶有最高的立体选择性,而物理吸附有最高的转化率。Ferreira等利用固定化南极假丝酵母脂肪酶B,在正己烷溶液中,能够选择性酰化一系列含呋喃和噻吩结构的外消旋二级醇。

